DNA 이중나선절단, 초기 복구 단계가 정교하게 조절되는 메커니즘 규명
유전체 항상성 연구단(단장 명경재, UNIST 바이오메디컬공학과 특훈교수) 이규영 연구위원(현 한림대학교 의과대학 교수) 연구팀은 가장 심각한 DNA 손상으로 알려진 ‘DNA 이중나선절단(Double-strand break)’의 초기 복구 단계가 정교하게 조절되는 메커니즘을 규명했다.
기초과학연구원(IBS) 유전체 항상성 연구단(단장 명경재, UNIST 바이오메디컬공학과 특훈교수) 이규영 연구위원(현 한림대학교 의과대학 교수) 연구팀은 가장 심각한 DNA 손상으로 알려진 ‘DNA 이중나선절단(Double-strand break)’의 초기 복구 단계가 정교하게 조절되는 메커니즘을 규명했다. 이 복구 과정에 문제가 있으면 유방암, 난소암 등을 일으킬 수 있다.
게놈 DNA는 생명 유지에 필요한 모든 정보를 가지고 있다. DNA 이중나선절단은 게놈 안정성을 위협하는 가장 위험한 DNA 상해 유형이다. 이에 대응하기 위해 우리 몸의 세포는 상동재조합 복구 시스템을 가동한다. 이 복구 시스템은 복구 결함과 돌연변이를 적게 발생시키며, 제대로 작동하지 않으면 세포가 사멸하거나 절단된 DNA가 다른 DNA 부위에 결합하는 등의 변형이 와 암을 유발할 수 있다.
상동재조합 복구는 여러 단계를 거치며, 각 단계는 다양한 복구 단백질에 의해 정교하게 조절된다. DNA 이중나선절단이 발생하면, MRN 단백질 복합체가 절단 인접 부위에 DNA 틈을 만들고, 틈을 기준으로 하여 양 방향으로 DNA 말단절제(End resection)가 일어난다.
말단절제는 절단 부위 말단에 결합해 있는 KU70/80 단백질을 제거해 향후 DNA 복구 합성의 시작점인 말단 부위를 드러나게 한다. 이후 DNA가 절제되면서 단일 가닥으로 노출된 말단 DNA는 정상의 상동 염색체 DNA에 침입해 상동 염색체의 상보적 DNA를 주형으로 하여 새로운 DNA를 합성한다.
* Ku70/80: Ku70과 Ku80 두 개의 단백질 복합체로, DNA 이중나선절단 말단에 결합해 말단을 구조적으로 지지 및 정렬하고, 말단을 보호한다.
연구팀은 이전 연구에서 암 억제 단백질 ATAD5가 상동재조합 복구 과정에서 핵심적인 역할을 수행하다는 사실을 밝혔다. 이번 연구에서는 상동재조합 복구의 초기 단계인 DNA 말단절제 과정에 DNA 복제 단백질 PCNA가 관여하며 ATAD5가 이를 조절한다는 것을 밝혔다. 말단절제는 후속 복구 시스템을 결정하는 동시에 후속 단계에 필요한 DNA 구조를 생성하는 핵심적인 기능을 한다.
* PCNA(Proliferating Cell Nuclear Antigen, 증식성세포핵항원) : DNA에 결합하여 DNA 합성을 돕는 단백질. DNA 합성 과정에서 여러 단백질을 끌어와 합성을 돕고, 이후 ATAD5에 의해 DNA와 분리된다.
* ATAD5(ATPase family AAA domain-containing protein 5) 단백질 : ATAD5 단백질은 4개의 단백질(RFC2,3,4,5)과 복합체를 형성하여 PCNA를 조절하는 복제 조절 단백질이다.
연구팀은 세포에 레이저를 조사해 특정 DNA 부위에 이중나선 절단을 유도한 뒤 형광 표지한 PCNA 단백질의 이동을 실시간으로 관찰했다. 그 결과, PCNA가 수십 초 내에 절단 위치에 나타나고, 일정 시간 이후에 사라지는 것을 확인했다.
연구팀이 MRN 단백질 복합체의 활성을 낮추자 PCNA가 감소하였으며, ATAD5의 양을 줄이면 PCNA가 오래 유지됐다. 이는 이중나선절단이 일어난 직후 MRN 단백질 복합체가 만든 DNA 틈에 PCNA 단백질이 신속하게 결합하고, 일정 시간이 지난 뒤 ATAD5에 의해 DNA에서 분리됨을 의미한다.
나아가 연구팀은 ATAD5가 제대로 역할을 하지 못하는 경우에 복구 결함과 게놈 불안정성이 나타나는 메커니즘도 규명했다. 정제 단백질을 이용한 생화학적․세포생물학적 실험을 통해 분석한 결과, 원활한 상동재조합 복구를 위해 말단절제가 진행 중인 DNA로부터 PCNA 분리가 필수였다. 분리되지 않고 남아 있는 PCNA는 DNA 틈으로부터 절단 부위 방향으로 진행되는 말단절제를 방해했다.
이는 후속 단계인 말단 결합 단백질 KU70/80 제거와 DNA 복구 합성을 저해하고, 전체적인 상동재조합 복구 빈도를 감소시켰다. 이렇게 상동재조합 복구가 어려운 상황에서, 세포는 오류를 유발하는 복구 시스템을 대안으로 선택해 생존을 이어간다. 하지만 이 선택은 결국 돌연변이 증가와 게놈 안정성 저하를 초래했다.
이규영 연구위원은 “상동재조합 복구의 후반 단계인 DNA 복구 합성 과정에서의 PCNA의 역할은 잘 알려져 있었다”라며, “이번 연구로 그간 밝혀지지 않은 복구 초기 단계에서의 PCNA의 역할과 중요성, 분자생물학적 조절 과정을 밝혔다”라고 말했다. 또한, “이번 연구성과는 상동재조합 복구에 문제가 있는 경우 발생할 수 있는 유방암 및 난소암 등에 대한 새로운 항암 전략 수립에 기여할 것으로 기대한다”라고 전했다.
이번 연구성과는 국제 학술지 ‘핵산 연구(Nucleic Acids Research)’에 9월 22일(한국시간) 온라인 게재됐다.
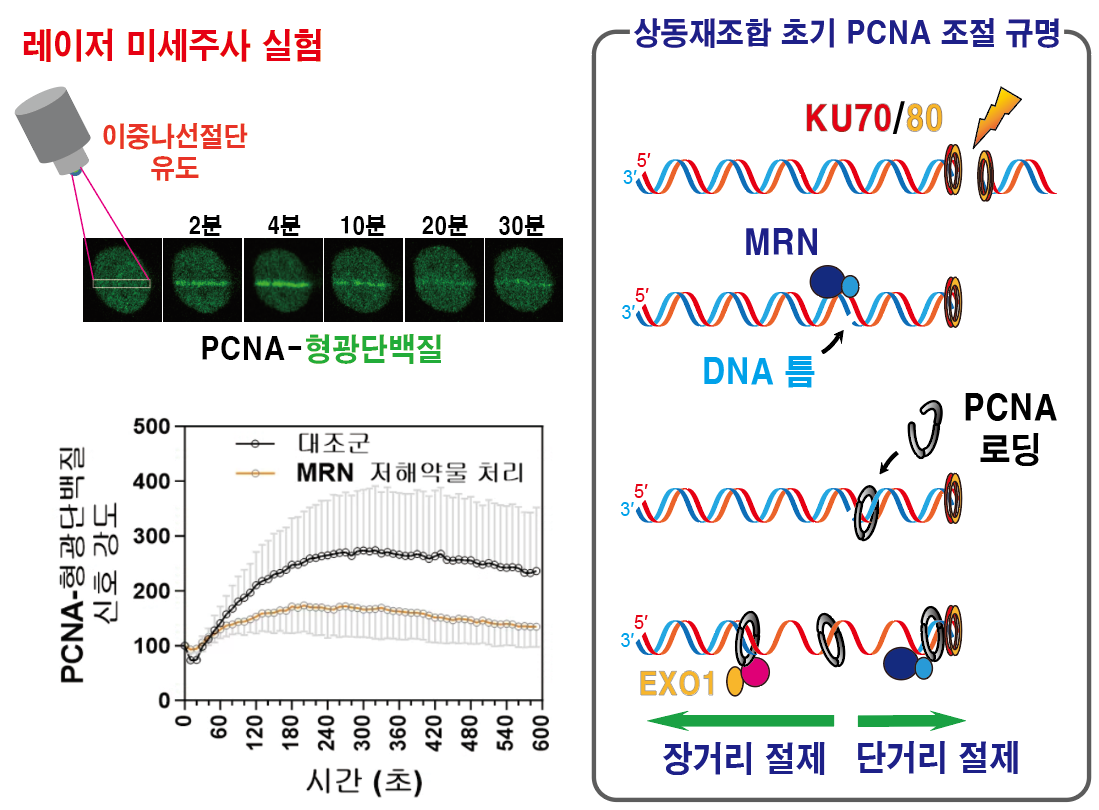
▲ DNA 이중나선절단 부위 인접 DNA 틈에 결합하는 PCNA
세포 내 지정된 위치에 DNA 이중나선절단을 유도하는 레이저 미세주사 실험(왼쪽 위 그림)에 의하면, PCNA는 절단 DNA에 신속하게 결합한다. PCNA 신호가 MRN 활성 저해 약물 처리 시에 감소하는 결과(왼쪽 아래 그림)는 PCNA가 MRN 단백질 복합체에 의해 형성된 DNA 틈에 결합함을 보여준다(오른쪽 그림).

▲ DNA 이중나선절단 부위에 남은 PCNA가 상동재조합 복구 결함을 일으키는 메커니즘
정상 세포(왼쪽 그림)에서 이중나선절단 부위 인접 DNA 틈을 통해 결합된 PCNA는 역할 수행 후 ATAD5에 의해 분리된다. 이후 말단 결합 단백질 KU70/80 제거를 포함한 상동재조합 후속 과정으로 이어진다. ATAD5 결핍 세포(오른쪽 그림)에서 이중나선절단 부위에 남은 PCNA는 단거리 말단절제를 방해해서 상동재조합 복구 결함으로 이어진다.
■ 연구 추가 설명
① 논문/저널/저자
Short-range end resection requires ATAD5-mediated PCNA unloading for faithful homologous recombination / Nucleic Acids Research (2023)
박수형, 김남우, 강나래, 류은진, 이은아, 라재선, Anton Gartner, 강석현, 명경재, 이규영
② 연구내용 보충설명
■ DNA 이중나선절단은 유전체 항상성을 위협하는 가장 위험한 DNA 손상 형태로, 상동재조합에 의한 무오류(error-free) 복구 과정이 매우 중요하다. 그 중요성은 상동재조합 복구의 핵심 단백질 BRCA 유전자의 돌연변이가 유전성 유방암 및 난소암의 원인이라는 것에서 알 수 있다. 실제로 2013년 미국 여배우 안젤리나 졸리가 본인이 보유한 BRCA 유전자 돌연변이와 암 가족력 등을 고려하여 선제적으로 유방을 절제한 사례가 국내에서도 화제가 되었다.
■ 이번 연구는 상동재조합 복구를 개시하는 첫 단계인 말단절제 과정에서 기존에 보고된 적이 없는 분자생물학적 현상 및 조절 과정, 그리고 그 중요성을 밝혔다.
③ 연구 이야기
[연구 과정]
■ 이번 연구는 레이저 미세주사(laser microirradiation) 실험을 통해 MRE11-RAD50-NBS1 핵산가수분해효소 복합체가 말단절제를 위해 생성한 DNA 틈(nick)에 PCNA가 매우 빨리 로딩(loading)되며, 이후에 이 PCNA가 다른 DNA 대사 과정에서와 유사하게 종양 억제단백질 ATAD5에 의해 DNA에서 분리된다는 것을 밝혔다.
■ 또한, 정제 단백질을 이용한 생화학 실험 및 세포생물학 실험을 통해, PCNA 분리가 제대로 안 되는 경우, DSB 말단 방향으로 일어나는 단거리 절제(short-range resec-tion)를 방해해서 말단 결합 단백질 KU70/80 제거에 문제를 일으키고, 결국 상동재조합 복구의 후반 단계인 DNA 복구 합성(repair synthesis)을 저해한다는 것을 밝혔다.
[성과 차별점 및 어려웠던 점]
■ 상동재조합 복구의 후반 단계인 DNA 복구 합성에서 PCNA의 역할은 수십 년 전부터 알려져 있었다. 이번 연구는 기존에 보고된 적 없는 상동재조합 복구 과정 초기 단계에 PCNA가 관여하고 있음을 새로운 밝힌 것이다. 새로운 연구내용을 제안하면서, 외부 발표나 논문 동료검토(peer-review) 시 다른 연구자들이 수용할 수 있도록 하는 과정에 많은 노력을 기울였다.
■ 사람 세포의 DNA 이중나선절단 복구 시스템은 상동재조합 복구를 포함해 총 4개가 있으며, 각 시스템의 세포 내 활성을 측정하는 방식이 다양하게 개발됐다. 측정 방식에 따라 직관적으로 예상되는 대로 결과가 나오지 않는 경우에는 각 측정 방식을 세부적으로 검토하고 그에 맞추어서 결과를 해석하는 데 많은 노력이 필요했다.
[향후 연구계획]
■ DNA 이중나선절단은 세포가 해결해야 할 심각한 손상이다. 그런데 일부 암세포에서는 DNA 이중나선절단이 노화와 관련된 텔로미어(telomere) 길이 유지 메커니즘의 시작 포인트로 작용한다. 향후 이 과정에 대한 연구를 심층적으로 진행할 계획이다.
■ 연구진 이력사항
<이규영 IBS 유전체 항상성 연구단 연구위원, 교신저자>

▲ 이규영 IBS 유전체 항상성 연구단 연구위원, 교신저자
1. 인적사항
○ 소 속 : IBS 유전체 항상성 연구단
(현 한림대학교 의과대학)
○ 전 화 : 010-3949-8946
○ e-mail : kylee@hallym.ac.kr
2. 학 력
1998 학사, 서울대학교
2000 석사, 서울대학교
2002 박사, 서울대학교
3. 경력사항
2006 – 2013 미국 국립보건원, 박사후연구원
2013 – 2015 LG 생명과학 신약연구소, 차장
2015 – 2023 IBS 유전체 항상성 연구단, 연구위원
2023 – 현재 한림대학교 의과대학, 부교수
<박수형 IBS 유전체 항상성 연구단 연구기술원, 공동 제1저자>

▲ 박수형 IBS 유전체 항상성 연구단 연구기술원, 공동 제1저자
1. 인적사항
○ 소 속 : IBS, 유전체 항상성 연구단 (현재 UNIST)
○ 이메일 : suhyung@unist.ac.kr
2. 학 력
2002 학사, 전남대학교
2004 석사, 전남대학교
2013 박사, 연세대학교
3. 경력사항
2013 – 2015 연세대학교, 박사후연구원
2015 – 2022 IBS 유전체 항상성 연구단, 연구기술원
2022 – 현재 울산과학기술원(UNIST), 연구조교수
<김남우 IBS 유전체 항상성 연구단 학생 연구원, 공동 제1저자>

▲ 김남우 IBS 유전체 항상성 연구단 학생 연구원, 공동 제1저자
1. 인적사항
○ 소 속 : IBS 유전체 항상성 연구단/UNIST
○ 이메일 : camphortreekim@unist.ac.kr
2. 학력
2018 학사, 울산과학기술원(UNIST)
2018 –현재 석/박사 통합과정, 울산과학기술원(UNIST)
3. 경력사항
2018 – 현재 IBS 유전체 항상성 연구단, 학생 연구원
출처: 기초과학연구원
기초과학연구원의 다른 포스터 인체 조직 경화증 진단 플랫폼 ‘나노 자성-버블’ 개발