‘테빔브라주’ 100밀리그램, 혁신적인 식도편평세포암 치료제 허가
“면역세포를 동원하는 ‘테빔브라주’, PD-1에 효과적으로 결합”
“식약처, 신약 ‘테빔브라주’ 허가로 식도편평세포암 치료 혁신”
“암 면역회피 방지, ‘테빔브라주’의 PD-L1 결합 방해 기작”
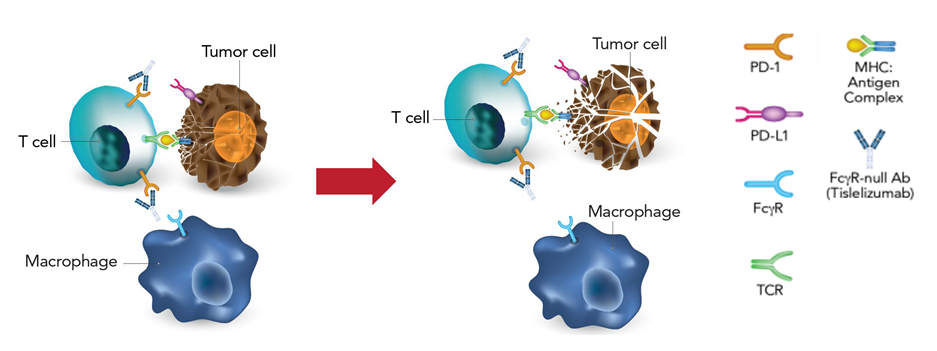
▲ 테빔브라주 작용기전(출처 : 업체자료 인용)
식품의약품안전처(처장 오유경, 이하 식약처)는 11월 20일 베이진코리아(유)(社)에서 개발한 새로운 식도편평세포암 치료제 ‘테빔브라주100밀리그램(티슬렐리주맙)’를 허가했다고 밝혔습니다.
이 신약은 면역관문 수용체로 알려진 세포예정사(PD-1)에 결합하는 단클론항체(mAb, IgG4)로, 식도편평세포암 환자에게 새로운 치료 기회를 제공합니다. PD-1은 활성화된 T세포, B세포, NK세포, 골수 계통 세포에서 발현되며 면역조절에서 중추적인 역할을 수행합니다.
* 세포예정사 1(programmed cell death 1, PD-1) : CD28 계열에 속하는 억제성 면역관문 수용체. 활성화된 T세포, B세포, NK세포, 골수 계통 세포에서 발현되며, 면역조절에서 중추적인 역할 수행
테빔브라주는 이전의 백금 기반 화학요법 치료를 지속할 수 없거나 투여 이후에 재발 또는 진행된 절제 불가능, 재발성, 국소진행성 또는 전이성 식도편평세포암 성인 환자에서 단독요법으로 사용됩니다.
암세포는 면역세포의 공격을 회피하기 위해 PD-L1을 표면에 발현시키고, 이 약은 PD-1과 PD-L1의 결합을 방해하여 면역세포가 암세포를 효과적으로 제거할 수 있도록 도와줍니다. PD-L1은 Programmed cell Death Ligand 1의 약자로, 암세포와 면역세포 간의 상호작용에서 중요한 역할을 합니다.
* PD-L1 : Programmed cell Death Ligand 1
식약처는 향후에도 규제과학을 기반으로 하여 안전성과 효과성이 확인된 치료제를 신속하게 공급하겠다고 밝혔습니다. 이번에 허가된 ‘테빔브라주’는 식도편평세포암 환자들에게 새로운 희망의 전망을 열어줄 것으로 기대됩니다.
전 세계적으로 암은 여전히 큰 건강 이슈로 여겨지고 있습니다. 특히, 식도편평세포암은 그 중에서도 치료가 어려운 양상을 보이는 암 중 하나입니다. 기존의 치료법이 한계를 보일 때, 새로운 치료제의 등장은 환자들에게 큰 소망이 될 수 있습니다.
테빔브라주의 등장은 PD-1에 특화된 효과적인 치료 기법으로 주목받고 있습니다. PD-1은 면역세포와 암세포 간의 상호작용에서 핵심적인 역할을 하는데, 이에 결합하는 테빔브라주는 암세포의 면역 회피 기전을 차단하여 면역세포가 암세포를 공격할 수 있게 합니다.
테빔브라주는 기존의 치료법이 무력해진 환자들에게 새로운 대안을 제시합니다. 이전에는 백금 기반 화학요법이 주로 사용되었으나, 이에 대한 내성이 발생하는 경우가 많아 새로운 치료제의 필요성이 대두되고 있습니다.
식약처는 허가된 치료제에 대해 안전성과 효과성을 철저히 검증하고 공급함으로써 환자들에게 안정적이고 효과적인 치료 기회를 제공하고자 합니다. 그동안의 연구 개발 과정에서 나온 테빔브라주가 환자들에게 실질적인 도움을 줄 수 있기를 기대합니다.
이러한 의약품의 허가는 암 치료 분야에서의 혁신적인 발전을 예고하며, 연구진과 기업들의 지속적인 노력이 치료법의 개선과 환자의 삶의 질 향상에 기여하고 있습니다. 앞으로도 안전하고 효과적인 치료제의 개발과 허가가 계속되어, 많은 환자들이 더 나은 치료 기회를 얻을 수 있기를 바랍니다.
출처: 식품의약품안전처